「有機フッ素化合物(PFAS)」評価書に関するQ&A(2025年7月18日)
初版:令和6(2024)年1月26日作成
第2版:令和6(2024)年2月6日更新
(Q2、Q5、Q6、Q8、Q10を更新)
第3版:令和6(2024)年2月13日更新
(Q7を更新)
第4版:令和6(2024)年6月25日更新
(Q6、Q7、Q9、Q10、Q11、Q12、Q13を更新)
第5版:令和7(2025)年3月19日更新
(Q14を追加)
第6版:令和7(2025)年7月18日更新
(Q10、Q14を更新、Q15〜Q17を追加)
本Q&Aは、食品安全委員会有機フッ素化合物(PFAS)ワーキンググループで審議し、パブリックコメントを経て、令和6年6月25日の第944回食品安全委員会においてとりまとめたPFASの食品健康影響評価書[PDF:7,528KB] に基づき、担当委員が作成したものです。
に基づき、担当委員が作成したものです。
情報提供(Q&A形式)の内容
I.評価の背景・手順・方法論
Q1 食品安全委員会は、なぜPFASの健康影響について自ら評価をしたのですか?
Q2 PFASの食品健康影響評価はどのような手順により行ったのですか?
Q3 食品健康影響評価(リスク評価)として、何を行ったのですか?
II.評価書の概要
(1)健康影響
Q6 ハザードの特性評価(PFASの健康への有害影響の性質と程度の評価)においては、どのような項目がどう評価されたのですか?
1)肝臓、脂質代謝
Q6-1 国外のリスク評価機関が健康影響に基づく指標値の算出に用いている血清ALT値や血清総コレステロール値の上昇について、どのように評価したのですか?
2)免疫毒性
Q6-2 ワクチン接種後の抗体価低下について、他国の評価で採用されているフェロー諸島での疫学研究をどのように評価したのですか?
3)発がん性
Q6-3 PFOSとPFOAの発がん性について、2023年に国際がん研究機関(IARC)が発表した分類結果を踏まえて、どのように評価したのですか?
(2)指標値
Q7-1 耐容一日摂取量(TDI)の設定の考え方やTDIの意味するところを教えてください。
Q7-2 米国や欧州のリスク評価機関では、疫学研究のデータが採用されていますが、今回のTDIは、国外のリスク評価機関が設定しているそれらの指標値と比較して高すぎるのではないでしょうか?
(3)摂取量
(4)血中濃度
(5)まとめと今後への課題
Q10 通常の一般的な食生活を送っている人たちへの影響について、食品安全委員会はどのように考えているのですか? 国内の高濃度汚染地域の住民の実態についてはどうなのでしょうか?
Q11 今回の評価書には、どのようなメッセージが込められているのでしょうか?
III.その他
IV.参考
評価書詳細:有機フッ素化合物(PFAS)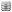
Q&A
I.評価の背景・手順・方法論
Q1 食品安全委員会は、なぜPFASの健康影響について自ら評価をしたのですか?
食品安全委員会は、これまで、食品や飲用水のほか、環境由来のばく露も考慮して、汚染物質の摂取による人の健康への影響についての評価やこれに向けた情報収集を行ってきました。この一環として、PFASについても、国内外の知見を収集し、関係機関に提供してきたところです。
その中で、近年、海外において、リスク評価及びリスク管理に関して新たな動きがあったことや、国内でも、厚生労働省及び環境省が水質の目標値等の検討を開始したことを受けて、まずはこれらの検討に資するような科学的な助言を行っていくべきとの考えに至りました。そのため、令和5年1月31日に、PFASを食品安全委員会が自ら行う食品健康影響評価(自ら評価※)の対象とすることを決定し、令和5年2月7日にPFASワーキンググループの設置を決定し、調査審議することとしました。
※ 食品安全委員会は、食品の安全を確保するため、食品に含まれる可能性のある様々な危害要因(ハザード)を摂取することによって起こる健康への影響についてのリスク評価(食品健康影響評価)を行っています。食品安全委員会が行うリスク評価には、新たな農薬を登録する場合などに厚生労働省、農林水産省等のリスク管理機関からの要請により行う評価のほか、自らの判断で対象案件を選定して行う評価(自ら評価)があります。
自ら評価の候補案件については、国民の健康への影響が大きいと考えられるもの、危害要因の把握の必要性が高いもの及び評価ニーズが特に高いと判断されるものの中から、リスク評価の優先度が高いと考えられるものを企画等専門調査会が選定し、国民からの意見・情報の募集を行った上で、食品安全委員会が決定しています。
Q2 PFASの食品健康影響評価はどのような手順により行ったのですか?
農薬等の食品健康影響評価においては、リスク管理機関からの依頼を受け、申請企業が提出したデータを中心に専門家が検討します。しかし、PFASは食品安全委員会が自ら、評価を行うことを決めたもので、かつ、意図せず食品に含まれる物質であるため、申請企業などはなくデータも提出されません。そのため、食品安全委員会は、PFASのうちPFOS、PFOA、PFHxSを中心に、国際機関や各国の政府機関が行った評価結果やそれに用いた知見を集めるために、令和4年度に調査事業を実施し、それによって関連する国内外の学術文献(計2,969報)を収集しました。これらの科学的知見に加えて、環境省、厚生労働省、農林水産省が実施した調査も考慮して、PFASワーキンググループが評価を行いました。また、各国の政府機関等が対象としなかった新型コロナウイルス感染症との関連を検討した新たな文献等も含め検討し、評価書(案)にまとめました。文献は、学術雑誌に掲載された査読※付き論文を用い、動物試験や疫学研究について、試験や研究の質も含めてPFASワーキンググループで議論しました(詳細はQ4参照)。
※ 論文が学術雑誌に掲載される前段階で、その分野の第三者の科学者等により、当該論文の科学的な妥当性、雑誌掲載の適否について審査(評価、チェック)をすること
Q3 食品健康影響評価(リスク評価)として、何を行ったのですか?
食品安全分野におけるリスク評価とは、食品に含まれる危害要因(ハザード)の摂取(ばく露)によるヒトの健康に対するリスクを、ハザードの特性等を考慮しつつ、付随する不確実性を踏まえて、科学的に評価することを指します。リスク評価は、通常、1)ハザードの特定(有害影響を及ぼす可能性がある物質等を特定)を行い、2)ハザードの特性評価(健康への有害影響の性質と程度を評価)を行います。また、3)ばく露評価(食品からハザードをどの程度摂取しているか推定)を行い、2)と3)の結果を用いて、4)リスク判定を行います。
(参照:農林水産省ウェブサイト)政府が適用する食品安全に関するリスクアナリシスの作業原則(CXG 62-2007)[PDF:189KB]
PFASの評価書においては、1)PFOS、PFOA及びPFHxSを対象として、2)動物試験の結果や、ヒトでの調査結果(疫学研究)から、どのような健康影響があるか、またどの程度の摂取量で起こり得るかを評価し、PFOS及びPFOAの耐容一日摂取量(TDI)を設定しました。また、3)これらの物質を食品や水を通じて日本人がどれくらい摂取しているかの情報を整理し、4)TDIと日本人の通常の一般的な食生活における摂取量を比較して、現時点におけるPFASワーキンググループの見解をまとめました。
Q4 評価書は、動物試験と疫学研究に大別して記述されています。どのような違いがありますか?
動物試験は、検討対象とする目的(確認したい毒性の種類)に応じて、用量等の試験条件の設計(動物種、性、一群あたりの動物数、投与経路、用量、投与期間、観察・検査項目等)を行うことが可能であり、多い量を投与して解剖なども行うことにより、影響を細かく検討することができます。そのため、ヒトでの影響を推測するために有用です。ただし、用いる動物とヒトとには種差があり、動物のデータをヒトに当てはめて類推すること(通常、ヒトへの外挿性、と表現されます)が妥当かどうかについては慎重に検討することが必要です。また、多くの場合、動物で見られる影響は、ヒトが現実にばく露し得る水準よりはるかに多い用量で試験した際の結果であることにも留意が必要です。
一方、疫学研究は、ヒトの集団における健康関連の様々な事象(疾病の発生等のアウトカム)の頻度と分布、それらに影響を与える要因を研究します。疫学の中に、横断研究や前向きコホート研究、後ろ向きコホート研究などがあります。疫学研究は、人間集団への化学物質のばく露によって生じる可能性のある健康影響についての有用な情報を提供し得るものですが、交絡要因※等から、真の関連とは異なった関連が観察されることがあります。疫学研究の結果の確からしさにも限界があることに留意が必要です。
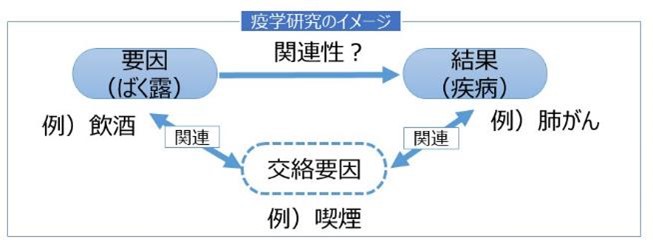
※ 例えば、飲酒と肺がんの関連を調べようとする場合、検討しようとする要因(飲酒)が、アウトカム(肺がんの発生)に影響を与える別の要因(喫煙)と密接に関連している(飲酒者は喫煙者でもあることが多い)ために、飲酒と肺がんの関連が正しく観察されない可能性があります。このとき、喫煙が交絡要因に該当し、喫煙が飲酒と肺がんの関連の検討に影響を与えないように、研究設計やデータ解析の段階で対策を講じる必要があります。
動物試験、疫学研究それぞれに特徴があり、評価において役立つ部分と手法上の限界となる部分の両方があります。また、双方共に複数の試験や調査が行われ、矛盾する結果が出ていることも少なくありません。そのため、評価書では、エンドポイント(有害影響を評価するための指標)ごとに、動物試験と疫学研究の結果についてそれぞれ、数多くの試験・研究の質や結果の一貫性などについて細かく検討した結果を記述し、それらをまとめた判断を記載しました。
Q5 評価において、日本人を対象とした研究結果はどの程度、取り入れられていますか?
今回の評価に際して収集された論文のうち、我が国における疫学研究の知見としては、北海道で進められている前向き出生コホート研究である「環境と子どもの健康に関するモニタリング調査(北海道スタディ)」が採用されています。この調査では、精神神経発達、アレルギー疾患などと生活環境や化学物質などの環境要因との関連について調査が行われています。
なお、今回のワーキンググループにおける議論には、この調査に携わっている研究者もメンバーとして加わっています。
II.評価書の概要
(1)健康影響
今回はハザードの特性評価は、以下の手順で行いました。
● PFOS、PFOA及びPFHxSの三物質を対象として、海外の評価機関等による評価書を参考に、以下に掲げる、エンドポイント(有害影響を評価するための指標となる生物学的事象)毎に整理検討
● エンドポイントごとの検討においては、健康影響についての指標値を設定するのに十分な証拠があるかどうかを吟味

※ 「限定的」、「不十分」とは
この評価書では、発がん性について、「限定的」とは、関連がみられたとする報告はあるものの、ほかに関連がなかったとする報告もあり、結果に一貫性がない場合「不十分」とは、関連がみられたとする報告はあるものの、症例数の規模が小さいなどから証拠としては不十分である場に用いられています。
他の健康影響についても、同様の考え方で検討したものの、「限定的」や「不十分」とは一概に分類できないものについては、その証拠の質や確からしさなどに応じた言葉が用いられています。
(参考)世界保健機関(WHO)傘下の一機関である国際がん研究機関(IARC)が2023年11月30日に発がん性の分類結果を公表しました。この分類は、PFOSやPFOAが発がん性を示す根拠がどれくらいあるかを示すものであり、発がん性の強さや摂取量による影響は考慮されていません。したがって、食品安全委員会が行う評価とは異なり、ヒトが実際の生活環境下で摂取(ばく露)したときに実際にがんが発生する可能性とその影響の程度(リスクの大きさ)を示すものでもありません。詳細は、「PFOA及びPFOSに対するIARCの評価結果に関するQ&A」を参照ください。
1)肝臓、脂質代謝
Q6-1 国外のリスク評価機関が健康影響に基づく指標値の算出に用いている血清ALT値や血清総コレステロール値の上昇について、どのように評価したのですか?
血清ALT値については、増加が見られても正常閾値内に収まる程度であり、かつ、のちに肝疾患につながることも示されていませんでした。また、PFASへのばく露が増加するに応じてALT値が増えるというような用量反応関係も不明確でした。
血清総コレステロール値については、複数の疫学研究で報告されているものの、ほとんどが横断研究であり因果関係が不明であること、研究間で結果が一致していないこと、血清総コレステロール値の増加の程度が軽微であること、のちに疾患につながることも不明であること、PFASのばく露が増加するに応じて血清総コレステロール値が増えるような用量反応関係は確認できなかった、という問題点があります。
特に、米国の高汚染地域での疫学研究では、血中PFAS濃度と血中ALT値やコレステロール値との関連が報告されているものの、血中濃度が高くなるほどALT値や血中総コレステロール値が直線的に高くなるわけではないため、耐容一日摂取量(TDI)のような指標値を算出することは困難であると判断しました。
2)免疫毒性
海外の評価機関で採用された文献のほとんどは、フェロー諸島で進められた研究ですが、フェロー諸島ではPFASの主なばく露源は鯨肉の摂食と考えられており、鯨肉の摂食によりPCBやダイオキシン類等の残留性有機汚染物質にもばく露されていること、フェロー諸島におけるPCBのばく露レベルは日本のデータに比べて約20倍程度高いことがわかっています。
また、フェロー諸島の研究を実施したグループは、母体血清PFASだけでなく、母体血清PCB濃度が高いと破傷風/ジフテリアの抗体価が低下することも報告しています。その一方で、血清PFAS濃度と血清PCB濃度は相関性があるとの報告もあり、ワクチン接種後の抗体価をエンドポイントとした場合のPFASばく露の影響とその他の残留性有機汚染物質ばく露の影響を切り分けた検証は行われていないことから、PFASの影響について評価するには情報が不十分であると判断しました。
3)発がん性
(2)指標値
Q7-1 耐容一日摂取量(TDI)の設定の考え方やTDIの意味するところを教えてください。
耐容一日摂取量(TDI:Tolerable Daily Intake)は、意図的に使用されていないにもかかわらず食品中に存在する物質について、ヒトが一生涯にわたって食品から摂り続けても健康に影響が出ないと推定される量のことです。体重1 kgあたりの物質の摂取量で示されます。
PFOS及びPFOAについて、現時点の科学的知見に基づくと、動物試験の結果から算出した健康影響に関する指標値として、TDIを、PFOS 20 ng/kg 体重/日、PFOA 20 ng/kg 体重/日とすることが妥当と判断しました。PFHxS については、評価を行う十分な知見は得られていないことから、TDIの算出は困難と判断しました。
なお、疫学研究の結果から報告がある影響については、現時点では、臨床的な意義が明らかになっていないことなどから、いずれもTDIなどの指標値を算出するには情報が不十分であると判断しました。
(参考)TDIの算出根拠
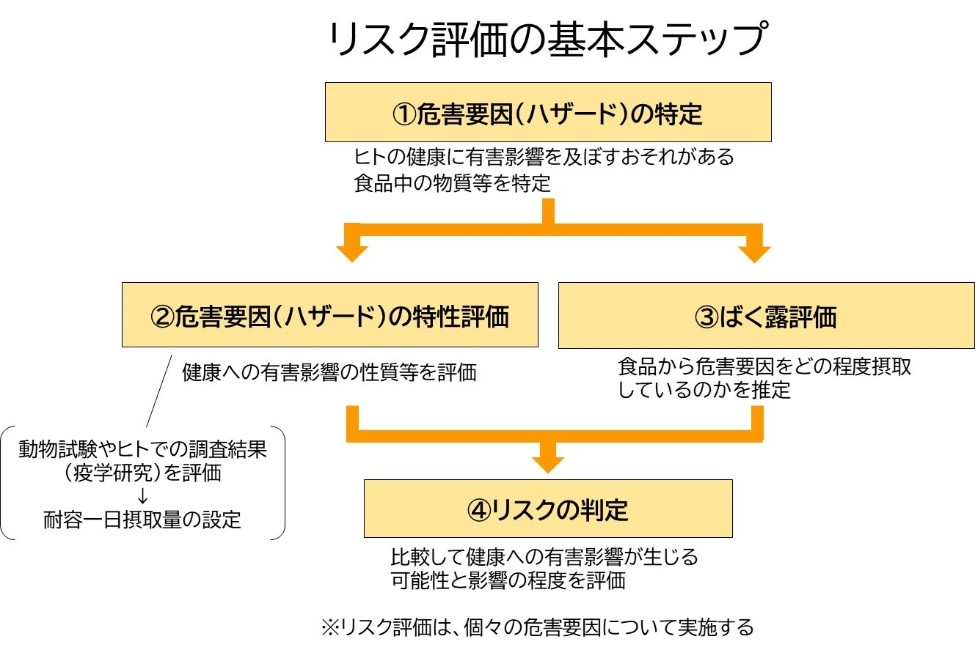
PFOS(20 ng/kg体重/日):ラットを用いた試験で児動物の体重増加抑制に基づき得られたNOAEL(0.1 mg/kg体重/日)を基に、ヒトの用量を推計するモデルから求めたPODHED※を不確実係数(30)で割って算出
PFOA(20 ng/kg体重/日):マウスを用いた試験で胎児の前肢及び後肢の近位指節骨の骨化部位数の減少等から得られたLOAEL(1 mg/kg体重/日)を基に、ヒトの用量を推計するモデルから求めたPODHEDを不確実係数(300)で割って算出
※ PODHED:ヒト等価用量に換算したPOD
米国や欧州のリスク評価機関が採用した疫学研究で報告されている血清ALT値の増加、血清総コレステロール値の増加、出生時体重の低下及びワクチンに対する抗体応答の低下については、いずれも数値の変化がみられる可能性は否定できないものの、
・血清ALT値の増加及び血清総コレステロール値の増加については、PFASばく露により影響がみられたとする報告もある一方で、職業的に高濃度ばく露を受けた人では影響がみられていない報告もあるなど結果の一貫性に課題があること、
・出生時体重の低下については、どの程度の摂取量(ばく露量)になるとどの程度の影響がみられるおそれがあるのか、また、どの程度の影響を「健康への悪影響」と捉えるのかについての情報が不十分であること、
・ワクチンに対する抗体応答の低下については、証拠の質や十分さに課題があること
から、それぞれ指標値を算出することは困難であると判断しました。
(3)摂取量
リスク評価では、「ハザードの特性評価」と並ぶステップとして「ばく露評価」を行います。そのため、日本人がどの程度PFASを摂取しているかを推定するため、関連する国内外の既存の知見を整理しました。
ヒトがPFASを摂取する経路としては、食品・飲料に加え、食品包装や粉じんからの経口摂取、カーペットや衣類等からの経口・吸入・経皮ばく露が指摘されています。
日本人の食品を通じたPFASの摂取については、限られた情報ではあるものの、2012-14年に農林水産省が実施した調査によれば、通常の一般的な食生活において推定されるヒト1日あたりのPFOSの平均的な摂取量は、0.60 ng/kg体重と1.1 ng/kg体重の間にあること、PFOAの平均的な摂取量は、0.066 ng/kg体重と0.75 ng/kg体重の間にあるとされました※。
この推定値は、今回の食品健康影響評価において現時点のデータおよび科学的知見に基づいて設定したTDIと比較すると低い状況にあるものと考えられます。
ただし、上記の推定値には、調査の実施年、調査点数、定量下限などに起因する不確実性があることに留意が必要です。国内における食品中のPFAS濃度に関するデータなど、現在の日本人の摂取量推定のための情報が不足しているため、ばく露実態の把握を進める必要があります。また、食品中のPFASの濃度については、試料 kg あたり ng のオーダーで非常に微量です。信頼できる分析結果を得るため、妥当性が確認された分析法に基づきデータが収集されることが重要です。
なお、上記の推定値は、欧州食品安全機関(EFSA)が公表した推定摂取量と比較すると、PFOSについては同程度、PFOAについては欧州よりも低い水準でしたが、調査手法や調査年次が異なることに留意が必要です。
※ 上記の日本人の平均摂取量は、通常の食生活における化学物質の平均的な摂取量を推定する手法であるトータルダイエットスタディにより算出されたものです。具体的には、地域ごとに幅広い種類の食品試料を購入し、食品群ごとに、食品群別消費量に比例するように混合した試料を調製し、食品群ごとにPFOS及びPFOAの濃度が分析されました。食品群別の濃度の平均値と日本人の食品群別の平均消費量を乗じて、それらを足し合わせることで日本人の平均的なPFOSやPFOAの摂取量が推定されました。
この調査が行われた当時の分析技術では、検出下限値(LOD)※1及び定量下限値(LOQ)※2が高く、多くの食品群において、PFOS及びPFOA濃度は、LODやLOQより低い結果でした。そのため、そのような食品群について、実際の濃度として推定される下限値(LOQ未満の分析値を0としたもの)を用いて計算した摂取量(LB)と、実際の濃度として推定される上限値(LOD未満の分析値をLODと同値、LOD以上LOQ未満の分析値をLOQと同値としたもの)を用いて計算した摂取量(UB)の双方の平均摂取量が示されています。実際の平均摂取量と比べて、摂取量(UB)は過大に、摂取量(LB)は過小に推定されている可能性があります。
※1 検出下限(Limit of Detection; LOD):ある分析法で化学物質を分析した場合に検出可能な最低濃度
※2 定量下限(Limit of Quantification; LOQ):ある分析法で化学物質を分析した場合に定量が可能な最低濃度
(4)血中濃度
ヒトの血中PFAS濃度は、過去のPFAS摂取を反映した値ですが、ヒトにおけるPFOS及びPFOAの消失半減期は数年にわたる長期間であり、体内動態については不確実な点が多いことから、測定された血中濃度の結果からPFASを摂取・ばく露した量、時期、期間等を推測することは現時点の知見では困難です。
今後のリスク評価に向けては、PFASの摂取量と血中濃度との関連や、それらと健康影響との関連について、疫学的手法により計画的に調査することが重要と考えます。
また、PFASばく露が懸念される地域の住民における血中濃度の分布、高ばく露者の把握等の必要性も含めて、今後のリスク管理の方策や対応の優先度等について検討することは重要と考えます。国や自治体等が、血中PFAS濃度測定を実施する場合は、その目的や対象者、実施方法、フォローアップの方法等について慎重に検討する必要があると考えます。
なお、米国科学・工学・医学アカデミーは、7つのPFAS分子種の合計として血清/血漿濃度が20 ng/mL超では健康影響のリスクが高まることをばく露患者へ伝えることを提言していますが、指標値を超過しても必ずしも健康影響を及ぼすものではないとしており、これは、ばく露の現状把握とその対策助言を目的としたリスク管理の観点からの提言であると考えます。
(5)まとめと今後への課題
今回、ばく露量推定で参照したデータは、複数の地域における食品を対象として推計した結果であることから、通常の一般的な国民の食生活から食品を通じて摂取される程度のPFOS及びPFOAによっては、著しい健康影響が生じる状況にはないものと考えられます。PFOS、PFOA等のリスクを過剰に懸念して食生活を変更することには、栄養学的な過不足をもたらす等の新たな異なるリスクをもたらすおそれがあります。
一方で、上記のデータには、調査地域数や定量下限の相違などに起因するかなりの不確実性があります。また、国内の各種食品中のPFAS濃度など摂取量の推定に関する情報が不足していることから、さらなる情報の集積を図っていく必要があります。
一般に、食品中の汚染物質のリスク管理については、「ALARA(as low as reasonably achievable:合理的に達成可能な限り低く)の原則」に従い、“無理なく到達可能な範囲でできるだけ低くすべき”とされています。
PFOS及びPFOAをはじめとするPFASについては、健康影響に関する情報が不足しており、不明な点等は多いものの、まずは、関係機関において、今回設定したTDIを踏まえた対応が速やかにとられることが重要です。そのためには、飲料水、食品等におけるデータの収集を早急に進め、こうした調査結果等をもとに、高い濃度が検出されたものに対する対応を進めることが必要です。
関係機関の取組状況については、Q17をご覧ください。
今般の食品健康影響評価、すなわちリスク評価は、科学的な知見・根拠に基づいて行ったものであり、リスク管理機関においては、リスク評価における不確実性や健康被害の「未然防止」等の観点も踏まえて、リスク管理の方策等が検討されるものと考えます。
評価書では、今後、リスク管理が迅速にかつ適切に行われるとともに、リスク管理に必要な科学的知見の収集がなされるよう、「まとめと今後の課題」の中で以下の内容を記載しています。
●まずは、リスク管理機関において
・今回設定したTDIを踏まえた対応が速やかに取られること
・PFASにばく露され得る媒体(飲料水、食品等)における濃度分布に関するデータの収集を早急に進めること
・その調査結果等をもとに、高い濃度が検出された媒体に対する対応等の対策を一層進めること
が重要と考えます。
●また、今後のリスク評価に向けて、PFASの摂取と健康影響との関連について、疫学的手法により計画的に調査することが必要であると考えます。
将来的に、今回の検討時には不十分であったPFASの健康影響に関する科学的な知見が集積してくれば、あらためて評価を実施する可能性はあると考えます。
PFOS、PFOA以外のPFASについては、個別の化合物ごとにリスク評価を行うための科学的知見は現時点では不十分であるため、研究・調査の充実が求められます。また、リスク管理機関においては、リスク評価における不確実性や健康被害の「未然防止」等の観点も踏まえて、リスク管理の方策等が検討されるものと考えます。
III.その他
1 PFAS、カドミウム、鉛等の汚染物質については、農薬のように評価ガイドラインにおいて評価に必要なデータセットが決まっていて、関係企業が試験を行ってデータを網羅的に揃えてリスク管理機関に提出し、それらがリスク管理機関から食品安全委員会に提出される、という体制にはなっていません。
したがって、汚染物質の評価では、最新の科学的知見を網羅的にカバーするため、まずは大学等の研究機関が実施した試験や調査結果についての文献を、学術論文のデータベース等で一定の検索条件で検索することになります。この段階では評価と関係の薄いものを含め、極めて多数の文献を収集します。
論文はアブストラクト(要旨)と本文から構成されていますが、極めて多数の論文の本文を全て精査することは膨大な作業であるため、続いてアブストラクトのみを読んで、評価書の作成に使用できる可能性がある文献に絞り込みます。
以後の評価の基点となるこの一連の作業は、調査事業として外部機関に委託して行っています。
2 食品安全委員会の専門調査会、ワーキンググループでは、調査事業で絞り込まれた文献リストをたたき台として、論文のアブストラクトだけでなく、本文及びそこに含まれるデータについて、専門家が精査します。この過程で、各国の評価機関が指標値を決定する際の根拠として用いた文献などの評価に必要であるにもかかわらず欠落していた文献などを追加することもあります。さらに、エンドポイントごとに、研究の質も考慮した上で、すべての論文を突き合わせ評価書としてまとめます。
このような過程を経て、評価書で引用、参照された文献(考え方を説明するために用いられた文献)が評価書の末尾に記載されます。評価においては、引用、参照された文献に限らず全ての文献を考慮していることに変わりはありません。
3 今回のPFAS評価に際しては、具体的には、以下のとおり文献選定を行いました。
(1)第1回ワーキンググループ会合において、
・「既にいろいろな国際機関が、それぞれ異なったエンドポイントに基づいて、異なった健康影響に関する指標値を出しておりますが、それについての知見を十分に吟味して評価していく」という大方針
・その後の作業として、エンドポイントごとに担当グループを作り、「分野ごとにどんな情報があって、どういう整理ができるのか、あるいはどういった情報が重要なのかという整理」からスタートする
ことを合意。(第1回ワーキンググループ(資料5、議事録))
(2) (1)に基づき、
a 調査事業で選定された257報のうち毒性評価に関するもの
b a以外のものであって、(1)の方針から当然必要となる米国環境保護庁(EPA)、欧州食品安全機関(EFSA)において、耐容一日摂取量等の設定の根拠とされた文献
c その他重要な情報として専門家により追加された文献をまとめたリストを作成し、これら一つ一つの文献についてデータを含めて全文を精査し、第2回ワーキンググループ会合に提出。エンドポイントごとの検討に当たり、なぜこれらの文献が必要なのか等についての議論を経て、これらを踏まえエンドポイントごとにドラフト(評価書の下書き案)の作成作業を開始することを合意(第2回ワーキンググループ(資料2−1、資料2−2、資料2−3。)
食品健康影響評価に用いる文献の選定プロセスはここで終了です。
4 なお、その後のワーキンググループ(第3〜9回)においては、内容を確認した全ての文献情報を踏まえ、エンドポイントごとにドラフトの作成を進める中で、そこで参照した文献について、末尾に一覧を記載します。これが、ドラフトの改訂ごとに繰り返されました。最終的な評価書案が合意された時点において、268の文献を参照文献として末尾に記載されましたが、先に述べたとおり、評価においては、引用、参照された文献に限らず全ての文献を考慮していることに変わりはありません。
注 なお、これらのPFASワーキンググループにおける議事録とそこでの議論の土台となった資料についてはWebサイト上で公開されており、これによって、上記3のとおりに手続きが進行したことを確認することが可能です。
(参考)
有機フッ素化合物(PFAS)ワーキンググループ
令和4年度調査事業報告書:パーフルオロ化合物に係る国際機関等の評価及び科学的知見の情報収集並びに整理
アブストラクト(要旨)を用い、評価書の作成に使用できる可能性がある文献(評価を進めていくためのたたき台)として、1)が整理されました。これに、各国の評価機関が指標値を決定する際の根拠として用いたものなど重要な文献が多数抜けていました。このため、1)にこれらを補ったうえで、その全てを用いて評価を進めました。さらに、健康影響についての指標値の設定に関する判断をより確実なものとするため、必要に応じ専門家が新たな文献収集も行いました。
このような過程で得られた科学的知見を統合して検討しまとめあげたものが評価書であり、評価書で引用、参照された文献等が2)として末尾に記載されています。
したがって、1)と2)は事実として別のものとなっています。
詳細は、Q14をご覧ください。
PFASの評価は、できるだけ速やかに進めなければならない、というのが食品安全委員会、ワーキンググループ双方の考えでした。しかし、評価は科学的に深い議論をしなければならず、その議論の土台となる資料の作成などの「準備」が必要です。そのため、ワーキンググループ開催にあたって、準備作業を行いました。
このため、準備作業における議事録は作成していません。
令和7年6月には、環境省が水道水の水質基準として「PFOS及びPFOAの合計値が50 ng/L以下であること」を新たに設定し、令和8年4月から、水道事業者等に対して、PFOS及びPFOAに関する水質検査の実施や基準を遵守する義務が新たに課されることになりました。
また、消費者庁がミネラルウォーター類のうち殺菌又は除菌を行うものに係る成分規格として「PFOS及びPFOAの合計値が50 ng/L以下であること」を設定し、令和8年4月から本規格に適合しなければならないことになりました。

