毒性及び毒性試験
リスクアナリシス(リスク分析)の考え方 / リスク評価 / 毒性及び毒性試験 / 疫学 / 分析・単位 / 化学物質系分野 /
生物系分野 / 新食品・栄養等分野 / 放射性物質 / リスクコミュニケーション / その他 /
用語一覧(50音順に検索) / 関係機関 / 関係法令 / 用語集のトップに戻る
■ 毒性及び毒性試験
ある物質が生体に有害影響を及ぼす性質をいう。
有害影響を評価するための指標となる、観察又は測定可能な生物学的事象。食品のリスク評価においては、通常、各種毒性試験において有害影響と判断される生物学的事象をエンドポイントとして、POD(Point of Departure)を設定する根拠とする。エンドポイントは必ずしも明らかな有害影響とは限らず、ばく露が増大すれば有害影響の発生につながる生理学・生化学的変化を指すこともある。毒性指標ともいう。
毒性影響をもたらす可能性がある物質の生体内への吸収、生体内での代謝、当該物質とその代謝物の生体組織への分布及び生体外への排出のプロセスをいう。
なお、標的部位におけるばく露条件(濃度及び時間)の下での、化学物質とその標的部位との相互作用及びその結果として生じる毒性影響をもたらす一連の反応をトキシコダイナミクス(Toxicodynamics)という。
化学物質の急性毒性の指標で、実験動物集団に経口投与等により投与した場合に、統計学的に、ある日数のうちに半数(50 %)を死亡させると推定される量(通常は物質量(mg/kg体重)で示す)のこと。LD50の値が小さいほど致死毒性が強いことを示す。
閾値が存在しない遺伝毒性発がん物質等の毒性に対し、生涯にわたり摂取した場合のリスクが、許容できるレベルとなるようなばく露量のこと。発がん性の場合、10万分の1あるいは100万分の1というような低い確率で発生させるばく露量となり、通常の生活で遭遇する稀なリスクと同程度の非常に低い確率となるようなばく露量(実質的に安全な量)と解釈される。
ある物質がどのように生体に作用する(望ましい効果、望ましくない効果又は副次的効果を与える)かを科学的に明らかにすることを目的とした試験のこと。
生物の遺伝情報を担う物質であり、デオキシリボース(糖)、リン酸及び4種類の塩基(アデニン(A)、グアニン(G)、シトシン(C)及びチミン(T))で構成される。DNAは二本鎖からなる分子で、一方の鎖のAと他方の鎖のT、また一方の鎖のGと他方の鎖のCが対合し、全体として二重らせん構造をとっている。この相補的二本鎖構造により、元のDNAを鋳型にしてコピーを作ることができ(DNAの複製)、生体内で一個の細胞が分裂して二個になるとき、複製されたDNA鎖が各細胞に分配され遺伝情報を伝えていく。
DNA上で遺伝情報を担う機能的・物理的構造。転写・翻訳される構造遺伝子とその発現を調節する調節遺伝子等がある。遺伝子は、多くの場合、タンパク質をコードするオープンリーディングフレームと発現を制御するプロモーター領域等からなる。
感染、病気又は望まない侵入生物を回避するために十分な生物学的防御力を持っている状態。病原体に一度感染すると、二度目からはかからない、又は、症状が軽減する等の異物に対する抵抗力を言う。現在では更に広い概念となっており、体内に自己の生存にとって不利益な病原体等が侵入したり、癌等が発生した場合に、これを選択的に排除しようとする機能であり、動物が生命維持のために備える基本的機能。
動物に繰り返し被験物質を投与した際にどのような毒性影響が生じるかの情報を得るための試験で、一般状態観察、体重や摂餌量の測定、血液学的検査、血清生化学的検査、尿検査、病理組織学的検査等を行う。
神経系への影響を判断するための試験で、実験動物を用いた試験法と培養細胞を用いた試験法がある。
実験動物を用いた試験では、被験物質を投与し、総合的な機能観察、電気生理学的検査、生化学的検査、神経病理組織学的検査等を行う。
化学物質等にばく露した後しばらく経過してから、運動、脊髄及び末梢神経における遠位軸索、神経組織におけるNTE(神経障害標的エステラーゼ)等に生ずる影響。
成熟雌ニワトリを用い、単回投与又は反復投与後に神経毒性兆候の観察、NTE活性の検査、神経病理組織学的検査を行う。
比較的短期間(通常1か月〜3か月程度)の反復投与によって生じる毒性のこと。亜慢性毒性(Subchronic Toxicity)ともいう。
化学物質などが生殖・発生の過程に有害な反応を引き起こすこと。
生殖毒性は親世代を中心に見ている(性成熟に達した動物の生殖能に悪影響を与え得る変化)一方、発生毒性は次世代を中心に見ている(発生・発育中の動物に対する悪影響)ものである。
ある物質の投与による、雌雄の生殖器系(生殖腺機能、性周期、交尾行動、受胎、妊娠、分娩、授乳及び離乳)、出生児の成長及び発達への影響に関する情報を得ることを目的として行う試験。交配前から物質の投与を開始し、交配、妊娠を経て次世代まで投与を継続し、親及び次世代への影響を調べる(2世代繁殖毒性試験の場合)。継代を行わない場合は1世代生殖毒性試験という。通常はラットを用いる。
ある物質の出生前等の投与による、妊娠動物と胎児に対する影響に関する情報を得ることを目的として行う試験。胎児の主要な器官が形成される時期に物質を投与した後、妊娠末期に子宮を摘出し、胚・胎児死亡、発育遅延、奇形発生等について調べる。通常、げっ歯類はラット、非げっ歯類はウサギを用いる(催奇形性試験を指すこともある。)。
妊娠中の母体にある物質を投与したときに、胎児に対して形態的、機能的な悪影響が生じる毒性のこと。
妊娠ラットに被験物質を投与し、神経病理組織学的検査、生まれてきた児動物の脳の発達、性成熟、学習能、運動量等の検査を行う。
物質が直接的又は間接的にDNAに変化を与える性質のこと。
細菌等の微生物、培養細胞又は実験動物を用いる方法があり、通常、いくつかの遺伝学的指標の異なる方法を組み合わせて、結果を総合的に評価する。変異原性試験ともいう。遺伝子突然変異試験や染色体異常試験等の変異原性試験とDNA損傷を検出するインディケーター試験(32Pポストラベル法やコメットアッセイ等)に分類される。
DNAや染色体に突然変異を引き起こす物理的、化学的、生物学的な作用をもたらす性質のこと。DNAに直接的又は間接的に変異をもたらし、細胞又は個体に影響を与える性質。
サルモネラ属菌又は大腸菌を用いて化学物質等を作用させて遺伝子(DNA)が突然変異を起こす頻度を調べる復帰突然変異試験(Reverse Mutation Test)のことで、変異原物質の第一次スクリーニング法としてブルース・エイムス博士が開発し、広く世界で用いられている試験。
遺伝毒性試験の一種で、ある物質によって誘発される生体内での染色体異常を細胞内の小核(※)の出現によって検出する試験。
※ 小核…遺伝子(DNA)に生じた切断が修復されずに残るために生ずる細胞核の断片で、遺伝子損傷の指標となる。
化学物質や放射線等の物理的要因の変異原性を調べる試験の一つ。化学物質や放射線等の作用により染色体の構造に重大な変化(染色体異常)が起こることがある。このような染色体異常を検出する方法としては、マウス等の実験動物や培養細胞を用いた染色体の形態的又は数的変化を観察する方法等がある。
化学物質が紫外線や可視光を吸収することにより活性化し、DNA損傷や突然変異を誘発し、その結果として発がん性を示すこと。
化学物質等が免疫系に悪影響を及ぼす性質。病原体や腫瘍細胞に対する抵抗性の低下を招く免疫系の抑制と、自己免疫疾患の悪化や過敏症(アレルギー)反応が引き起こされうる免疫系の亢進(こうしん)がある。
ある化学物質がアンドロゲン(男性ホルモン)様作用を有するかどうかをin vivoでスクリーニングする試験。去勢した雄ラットに被験物質を投与し、アンドロゲン依存性組織(精嚢、腹側前立腺等)の重量増加を検討する。
ある化学物質がエストロゲン(女性ホルモン)様作用を有するかどうかを確認する試験。未成熟雌又は卵巣を摘出した雌ラットに被験物質を投与し、エストロゲン依存性組織である子宮の重量増加を検討する。
ある動物の染色体に他の生物の遺伝子(DNA)を人為的に挿入し、その遺伝子により新しい性質や能力を持った動物のこと。このような遺伝子組換え動物は、医学領域等の研究のためにヒトの病気と同じ症状を発症させたマウスや、安全性評価における化学物質等の変異原性を調べることができるマウス等の実験動物として既に利用されている。また、肉・乳等の畜産物の生産性の向上、家畜の病気に対する抵抗性の付与、医薬品原料等の有用物質の生産等を目的とした遺伝子組換え動物の開発が進められている。
ある遺伝子機能の発現を欠損させたマウスをノックアウトマウスといい、遺伝子欠損マウス、遺伝子ターゲッティングマウスともよばれる。
特定の遺伝子を、染色体上の特定の位置に導入されたマウスのこと。例えば、ある変異を入れた遺伝子を導入することにより、個体レベルで変異の影響を確認することができる。
生体に作用してがんを発生させる性質のこと。
食品健康影響評価における発がん性試験は、良性腫瘍と悪性腫瘍の双方を対象として評価する。
化学物質や放射線等によって遺伝子(DNA)に損傷が起き、修復されずに突然変異として遺伝子に固定される発がんの最初のステップをいう。ただし、この作用だけでがんになるとは限らない。
発がんの「促進」、「助長」という意味。プロモーション作用だけでは必ずしもがん化しないが、イニシエーション期に遺伝子変異を起こした細胞を増殖させ、がん化に導く作用のこと。
遺伝子(DNA)に損傷を起こし遺伝子の突然変異を起こす物質で、イニシエーション作用を有し発がんの最初の原因となる物質を指す。また、多くはプロモーション作用も有していると考えられている。
国際がん研究機関(IARC)が、ヒトに対する発がん性に関する様々な要因(化学物質、ばく露環境等)を評価し、4段階に分類したもの。各要因が発がん性のあるハザード(cancer hazard)であるかどうかについて、入手可能な証拠の強さを評価し分類するものであり、発がん性の強さや発がんリスク(cancer risk)の大きさを示すものではない。
なお、IARCは、「発がん性のあるハザード」は、発がんの原因となりうる因子のことであり、「発がんのリスク」は、発がん性のあるハザードへの一定程度のばく露を前提とした場合にがんが起きる蓋然性としており、ハザードとリスクの区別は重要である、と説明している。
|
グループ
|
評価内容
|
例
|
|---|---|---|
|
1
|
Carcinogenic to humans
(ヒトに対して発がん性がある) |
コールタール、アスベスト、たばこ、カドミウム、ベンゾ[a]ピレン、ディーゼルエンジンの排気ガス、アルコール飲料等
|
|
2A
|
Probably carcinogenic to humans
(おそらくヒトに対して発がん性がある) |
アクリルアミド、エピクロルヒドリン、クレオソート(木材の防腐剤)、非常に熱い飲み物(65℃以上)、ヒドラジン等
|
|
2B
|
Possibly carcinogenic to humans
(ヒトに対して発がん性がある可能性がある) |
ベンゾフラン、フェノバルビタール、わらび、ガソリン等
|
|
3
|
Not classifiable as to its carcinogenicity to humans
(ヒトに対する発がん性について分類できない) |
カフェイン、お茶、コレステロール等
|
(参照)IARC Monographs on the Identification of Carcinogenic Hazards to Humans:CLASSIFICATIONS
https://monographs.iarc.fr/agents-classified-by-the-iarc/
ある物質を動物に投与して、その物質の体内動態(吸収、分布、代謝、排泄等)に関する科学的知見を得るための試験のこと。動物体内運命試験、薬物動態試験ともいう。
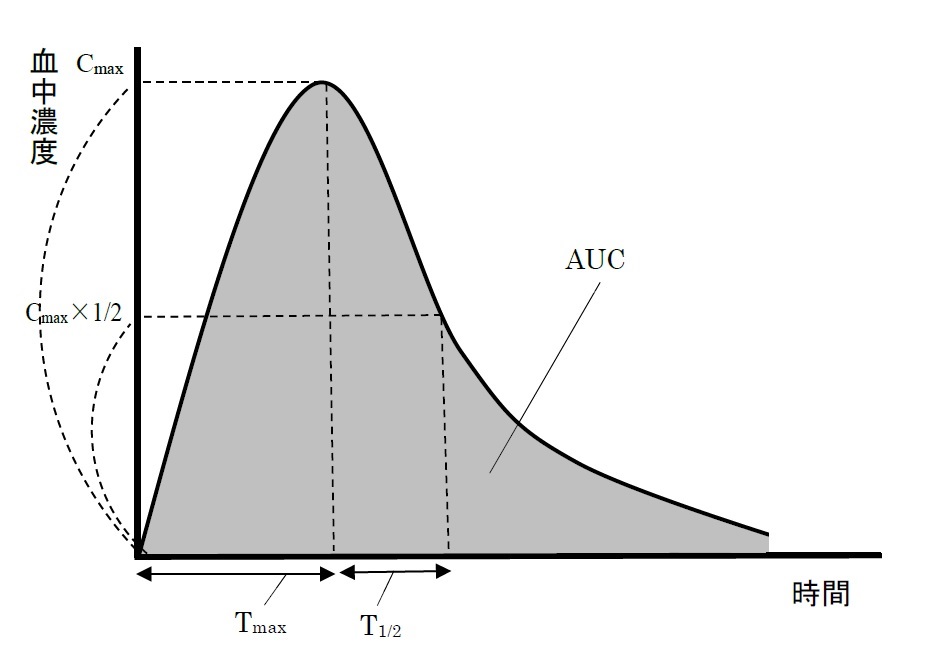
(参考)体内動態試験で使用される指標
・Cmax:最高血中濃度
ある物質の投与後、その物質の血中濃度が最高点に達したときの濃度
・Tmax:最高血中濃度到達時間
ある物質の投与後、その物質の血中濃度が最高点に達するまでの時間
・T1/2:血中濃度半減期
ある物質の投与後、その物質の血中濃度がCmaxに達してから半分に減少するまでの時間
・AUC(Area Under the blood concentration time Curve):血中濃度−時間曲線下面積(血中濃度曲線下面積)
投与した物質の血中濃度の時間経過を表した曲線と横軸(時間軸)によって囲まれた部分の面積。物質が生体にどの程度吸収されたか、又は生体が物質にどの程度ばく露されたかを示す指標となる。
化学的ハザード(親化合物)にばく露された植物又は動物の体内で、親化合物が代謝を受け生成された化合物をいう。親化合物と共に、リスク評価の対象として考慮され得る。
投与された化学物質が全身循環に到達する割合。生物学的利用能ともいう。
なお、栄養学においては、摂取された栄養素が利用される程度を示す値であり、栄養素の吸収効率と体内で利用される効率を併せて評価したもの。
化学物質の投与等による変化のうち、生体の恒常性が維持されている範囲において起こる器官や組織の変化。化学物質の毒性評価においては、恒常性の範囲を超え有害影響が認められる場合は適応性変化に含まれない。

