アスパルテームに関するQ&A
2023年7月13日公開
(背景情報説明)
2023年7月19日更新
(各組織の評価結果説明とリンク先の追加等)
甘味料のアスパルテームについて、世界保健機関(WHO)傘下の一機関である国際がん研究機関(IARC)が発がん性を、FAO/WHO合同食品添加物専門家会議(JECFA)が実際に摂取した際の健康への影響を評価し、その結果を2023年7月14日、公表しました。IARCは、アスパルテームの発がん性をグループ2Bに分類、JECFAは前回(1981年)の評価の際に設定した許容一日摂取量(ADI)を変更する理由はない、としました。
アスパルテームへの社会の関心が高いことから、食品安全委員会は、IARCやJECFAが行った評価について、その結果や意味をQ&A形式で整理し、情報提供することにしました。
今後とも、IARC及びJECFAが公表する情報を見ながら、必要があれば、本ウェブページを更新します。
情報提供(Q&A形式)の内容
1-1 今回のIARCの評価結果は?
1-2 IARC発がん性分類は何を示しているのか?
1-3 IARCが分類する4つのグループとは?
1-4 今回IARCが、アスパルテームの発がん性分類を「グループ2B」とした根拠は?
2-1 今回JECFAが行った評価の概要は?
2-2 JECFAや食品安全委員会が行う「リスク評価」とは、何を行うのですか?
3 JECFAとIARCの評価の違いは何か?
4 アスパルテームの長期発がん性試験結果をめぐるこれまでの海外当局の評価状況を教えて欲しい。
5 これまでのアスパルテームに関する国内の評価結果は?
6 日本でのアスパルテームの摂取量はどの程度か?
7 WHOが2023年5月に発表したノンシュガー甘味料の使用に関するガイドラインについて概要を教えて欲しい。
8 WHOが2022年4月に公表したノンシュガー甘味料の使用による健康影響に関する報告書について概要を教えて欲しい。
Q&A
Q1-1 今回のIARCの評価結果は?
「IARCは、アスパルテームの発がん性について、4つの発がん性分類のうち「グループ2B」と評価しました。
IARCの発がん性分類は、様々な要因(化学物質、微生物、作業環境や特定の行為等)について、ヒトに対する発がんの原因となり得るかどうかの根拠の強さを示すものです。この分類は、各要因の発がん性の強さを示すものではありません。また、各要因に現実的なレベルでばく露したときに実際にがんが発生する可能性の大きさを示すものではありません。
(参考)IARC Monographs Q&A
Q1-3 IARCが分類する4つのグループとは?
IARCは、各要因について、以下の(1)〜(3)に関する入手可能なデータを評価し、人に対する発がん性の根拠の強さに応じて4段階(1、2A、2B、3)に分類しています(表1を参照)。
(1) 人に対する発がん性(ヒトの疫学研究)
(2) 動物に対する発がん性(ラットやマウスなどの動物試験)
(3) 発がんの機序(発がん性物質としての主要な特性を示すかどうかの試験)
| グループ | 評価内容 | 発がん性を示す根拠の程度 |
|---|---|---|
| 1 | Carcinogenic to humans (ヒトに対して発がん性がある) |
・ヒトにおいて「発がん性の十分な証拠」がある場合 または ・実験動物において「発がん性の十分な証拠」があり、かつ、ヒトにおいて発がん性物質としての主要な特性を示す有力な証拠がある場合 |
| 2A | Probably carcinogenic to humans (おそらくヒトに対して発がん性がある) |
以下のうち少なくとも2つに該当する場合 ・ヒトにおいて「発がん性の限定的な証拠」がある ・実験動物において「発がん性の十分な証拠」がある ・発がん性物質としての主要な特性を示す有力な証拠がある |
| 2B | Possibly carcinogenic to humans (ヒトに対して発がん性がある可能性がある) |
以下のうち1つに該当する場合 ・ヒトにおいて「発がん性の限定的な証拠」がある ・実験動物において「発がん性の十分な証拠」がある ・発がん性物質としての主要な特性を示す有力な証拠がある |
|
3 |
Not classifiable as to its carcinogenicity to humans (ヒトに対する発がん性について分類できない) |
上記いずれにも該当しない場合 |
これまで、IARCは合計で1042の要因を評価し、そのうち126要因(例:たばこ、アルコール飲料)について、ヒトにおける発がん性を示す有力な根拠があると判断し、グループ1(ヒトに対して発がん性がある)に分類しています。2A、2B、3となるにつれて、ヒトにおける発がん性の根拠は弱くなります。
グループ2A(おそらくヒトに対して発がん性がある)には94要因が分類されています。主に、動物試験において発がん性を示す有力な根拠があり、ヒトにおける発がん性を示し得る一定の根拠があるものの決定的ではないものが該当します。より発がん性の根拠が弱いグループ2B(ヒトに対して発がん性がある可能性がある)には322要因が分類され、主に、動物試験において発がん性を示す有力な根拠があるものの、ヒトにおける発がん性を示す情報がない又はほとんどないものが該当します。
残りの500要因(全体の約半数)は、グループ3(ヒトに対する発がん性について分類できない)に分類されています。グループ3は、発がん性がないことを示すわけではなく、主に、発がん性の有無を判断するためのデータが不足しているものが該当します。
IARCの発がん性分類は、人に対する発がん性を示す根拠の強さを示すものであり、一定量ばく露した際にどの程度がんが発生する可能性があるかを示すものではありません。同一グループ内のある要因と別の要因とでは、発がんの可能性や程度は異なるため、両者を比較することは適切ではありません。
| グループ | 評価内容 | 要因の数 | 例 |
|---|---|---|---|
| 1 | Carcinogenic to humans (ヒトに対して発がん性がある) |
126 | コールタール、アスベスト、たばこ、カドミウム、ディーゼルエンジンの排気ガス、アルコール飲料等 |
| 2A | Probably carcinogenic to humans (おそらくヒトに対して発がん性がある) |
94 | アクリルアミド、非常に熱い飲み物(65℃以上)、ヒドラジン、夜間勤務 等 |
| 2B | Possibly carcinogenic to humans (ヒトに対して発がん性がある可能性がある) |
322 | ベンゾフラン、フェノバルビタール、わらび、漬物、ガソリン等 |
| 3 | Not classifiable as to its carcinogenicity to humans (ヒトに対する発がん性について分類できない) |
500 | カフェイン、お茶、コレステロール等 |
IARCは、3つの要件(Q1-3表1参照)の全てにおいて限界があるとしつつ、以下の理由から、4グループのうち、2B(ヒトに対して発がん性がある可能性がある)と分類しました。
- ノンシュガー甘味料(artificial sweetener)を用いた飲料とヒトの肝臓がんの関係を調べ、両者に正の相関があるとする3つの研究報告があるが、これらの研究においても全体又は一部の重要な集団において、偶然性、バイアス又は交絡因子は排除できないこと、
- マウス及びラットを用いた試験で、雌雄ともに腫瘍が増加したという3つの報告があるが、試験設計及びデータの解釈等に疑義があることから、実験動物における発がんの証拠は限定的と結論したこと、
- アスパルテームが発がん性を示すというメカニズムに関する証拠が限られていること。
Q2-1 今回JECFAが行った評価の概要は?
JECFAは、アスパルテームについて、IARCが評価の対象とした試験動物やヒトのデータも含めて評価した結果、以下に示す理由から、1981年の評価の際に設定した許容一日摂取量(ADI):0-40 mg/kg 体重/日を変更する理由はなく、このADIが適切であることを確認しました。
- アスパルテーム摂取が、発がんやそれ以外の影響を含め、ヒトに有害な影響を与えるという確たる証拠はなかったこと
- アスパルテームは、摂取後に消化管内で分解され、一般的な食品を摂取した後に吸収される代謝物と同じ物質(フェニルアラニン、アスパラギン酸、メタノール)となり、アスパルテームがそのまま全身循環に入ることはないこと
また、世界各国におけるアスパルテームの一日当たりの経口摂取量を推定したところ、摂取量※はADIより低かったことから、アスパルテームの摂取により健康への悪影響が生じる懸念はないと述べています。
世界での多食者の摂取量:大人 ≦12 mg/kg 体重、子ども ≦20 mg/kg 体重
許容一日摂取量(ADI):ヒトが一生涯にわたって毎日摂取し続けても、健康への悪影響がないと考えられる1日当たりの物質の摂取量
食品安全分野におけるリスク評価とは、食品に含まれるハザード(危害要因:人の健康に有害影響を及ぼす可能性がある生物的、科学的及び物理的な要因・物質)の摂取(ばく露)によるヒトの健康に対するリスクを、ハザードの特性等を考慮しつつ、付随する不確実性を踏まえて、科学的に評価することを指します。
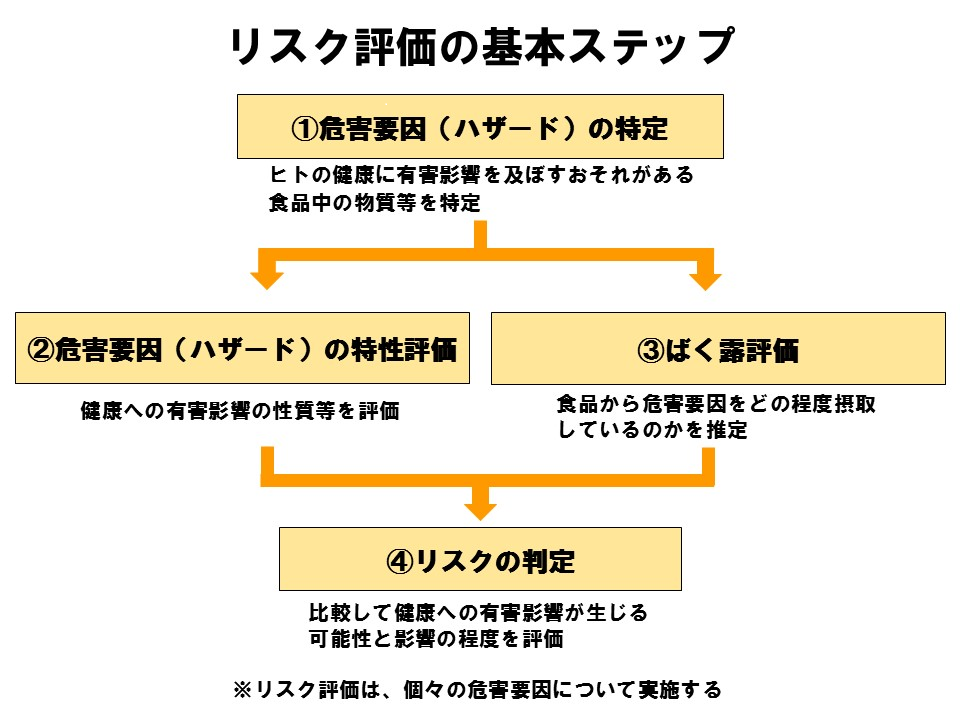
政府が適用する食品安全に関するリスクアナリシスの作業原則(CXG 62-2007)によれば、リスク評価は、1)ハザードの特定、2)ハザードの特性評価、3)ばく露評価、4)リスク判定の4つの段階を含むべきであるとされています。それぞれの内容は以下の通りです。
1) ハザードの特定
特定の食品又は食品群中に存在する可能性があるハザードを特定し、それらについての既知の科学的情報を整理します。
2) ハザードの特性評価
摂取されたハザードに起因して生じる健康への有害影響の性質と程度を定性的及び/又は定量的に評価します。食品添加物などの化学的な要因については、用量反応評価を実施し、これに基づき、健康影響に基づく指標値を設定します。
3) ばく露評価
人が食品を通じてハザードをどの程度摂取しているのか、定性的及び/又は定量的なデータから推定すること。食品中のハザードの含有量や食品の摂取量等から現実に近い摂取量を算出します。
4) リスク判定
ハザードの特性評価とばく露評価に基づき、ある集団における既知の、又は今後起こりえる健康への有害影響が生じる可能性とその程度について、付随する不確実性を含めて評価します。
IARC は、物質や作業環境などの様々な要因の発がん性をグループ1、2A、2B、3の4段階に分類しています。
ただし、この分類は、がんを引き起こす可能性に関する科学的証拠の強さを示したものであり、発がん性の強さやばく露量による影響が考慮されていないことから、人における実際の発がんの確率や重篤性を示すものではありません。
IARC自身も、「発がん性を理解するための最初の基本的な段階であるハザード特定を行う」と述べています。
その物質が実際の生活環境下において人に対して健康への悪影響を及ぼすかについては、JECFAや食品安全委員会が行っているように、「ハザード特定」に加えて「ハザード特性評価」や「ばく露評価」も合わせた、リスク評価を行う必要があります。この際、JECFAや食品安全委員会は、発がん性以外の消化吸収代謝への影響や生殖毒性などさまざまな有害影響にも着目して、リスク評価を行います。
さらに詳しく知りたい方は、こちら(リスク評価と国際がん研究機関(IARC)の発がん性評価について(リンク))をご覧ください。
欧州食品安全機関(EFSA)は、アスパルテームについての再評価結果を2013年に公表しています。2002年に行われたEU食品科学委員会(SCF)で設定された許容一日摂取量(ADI)40 mg/kg 体重/日について、安全上の懸念はなく、ADIを変更する必要はないとしています。
SCFがADIを設定した後、欧州ラマツィーニ財団(ERF:European Ramazzini Foundation of Oncology and Environmental Sciences)が、アスパルテームの発がん性を示すものとしてラットを用いた2つの試験結果(2006年及び2007年)とマウスを用いた試験結果(2010年)を学術論文として発表しました。しかし、EFSAの再評価レポートは、方法論的欠陥があると結論づけています。
米国食品医薬品庁(FDA)は、ERFにより 2005 年に発表された発がん性に関する研究について検討し、2007 年に「FDA Statement on European Aspartame Study」として公表しています。FDA は、食品の一般的な甘味料としてのアスパルテームのADI=50 mg/kg 体重/日を変更する理由はないと結論づけています。
海外機関の情報について、より詳細は、国立医薬品食品衛生研究所安全情報部が作成している「食品安全情報 」を参照してください。
」を参照してください。
日本では1983年、厚生省(当時)がアスパルテームを食品添加物に指定しており、その際、JECFAが設定していたアスパルテーム及び分解生成物であるジケトピペラジンのADI、それぞれ40 mg/kg 体重/日及び7.5 mg/kg 体重/日を採用しています。
食品安全委員会では、令和4年度に実施した「食品添加物の海外の評価結果等に関する情報収集及び調査」において、アスパルテーム等の甘味料3品目と安息香酸等の保存料2品目について、文献情報や海外での評価情報を収集・整理して、品目概要及び選定した文献についての有識者の査読コメントを公表しています。
文献情報については、関連のキーワードを元に文献検索をした結果から有識者の意見を踏まえ、アスパルテームについては143報の文献を選定・収集しました。そのうちERFの論文を含め8報の文献については、有識者の査読コメントを掲載しています。特にERFの論文については、海外機関の評価と同様、動物が終生飼育のため、種々の要因が動物に負荷としてかかっている可能性があるなど、試験デザインの問題が指摘されており、現在の情報では種々の疑問点があり、論文から得られる情報は限定的であるとしています。
食品安全委員会 食品添加物の海外の評価結果等に関する情報収集及び調査
https://www.fsc.go.jp/fsciis/survey/show/cho20230030001
厚生労働省は毎年度、食品添加物を選びマーケットバスケット方式による摂取量推計調査を実施しています。最近約10年では、アスパルテームについては以下の結果が公表されています。
<成人1人あたりの推定摂取量と対ADI比(ADIは40 mg/kg 体重/日)>
・2011年度 混合群一日推定摂取量 0.019 mg/人/日、 対ADI比0.001%
・2015年度 混合群一日推定摂取量 (混合群中の濃度が定量下限未満のため算出せず)
・2019年度 混合群一日推定摂取量 0.055 mg/人/日、 対ADI比0.002%
令和4年度の厚生労働科学研究「生産量統計調査を基にした食品添加物摂取量の推定に関わる研究」では、生産量統計調査による推計値結果としてアスパルテームの一人あたりの一日摂取量の推計結果が公表されています。
アスパルテーム 6.58 mg/人/日 対ADI比0.3%
いずれの調査結果でも、推定摂取量はADIよりも大幅に低い値です。
(参考)厚生労働省 マーケットバスケット方式による年齢層別食品添加物の一日摂取量の調査
https://www.mhlw.go.jp/stf/seisakunitsuite/bunya/kenkou_iryou/shokuhin/syokuten/sesshu/index.html
令和4年度厚生労働科学研究費補助金(食品の安全確保推進研究事業)「食品添加物の試験法の検討及び摂取量に基づく安全性確保に向けた研究」報告書
https://mhlw-grants.niph.go.jp/system/files/report_pdf/202224027A-sonota1.pdf[PDF形式:2,507KB]
国立医薬品食品衛生研究所安全情報部が作成している「食品安全情報」で、当該ガイドラインの内容について、紹介されています。
http://www.nihs.go.jp/dsi/food-info/foodinfonews/2023/foodinfo202311c.pdf[PDF:840KB]
食品安全委員会が公表している「食品安全情報」で、当該ガイドラインの内容について、紹介されています。
https://www.fsc.go.jp/fsciis/foodSafetyMaterial/show/syu05820610294
(参考)ノンシュガー甘味料使用の健康影響:系統的レビューとメタアナリシス(2022年4月)
Health effects of the use of non-sugar sweeteners: a systematic review and meta-analysis
World Health Organization, Rios-Leyvraz, Magali & Montez, Jason. (2022)
https://iris.who.int/handle/10665/353064

